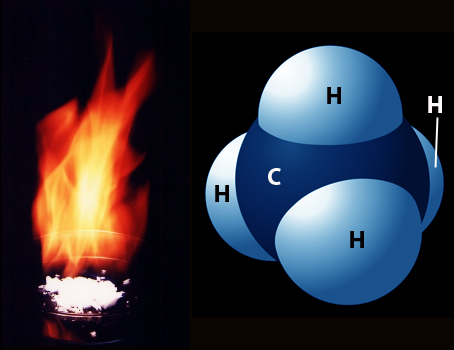
ก๊าซมีเทน (CH4) เป็นสารไฮโดรคาร์บอนอิ่มตัวประเภทอัลเคน (alkane) หรือ พาราฟิน (paraffins) ที่ได้จากกระบวนการย่อยสลายอินทรีย์วัตถุของจุลินทรีย์แบบไม่ใช้ออกซิเจน
ก๊าซมีเทน เป็นก๊าซเรือนกระจก 1 ใน 6 ชนิด ที่ก่อให้เกิดปัญหาโลกร้อนหรือภาวะเรือนกระจก (Green House Effect) ได้มาก มีช่วงอายุในบรรยากาศประมาณ 10 ปี มีศักยภาพทำให้โลกร้อนเป็น 25 เท่าของก๊าซคาร์บอนไดออกไซด์ เนื่องจากสามารถสะท้อน และดูดกลืนรังสีความร้อนได้ดีกว่าก๊าซคาร์บอนไดออกไซด์ พบเกิดมากในแหล่งเกษตรกรรม โดยมีเขตนาข้ามเป็นอันดับ 1 และรองลงมาเป็นเขตปศุสัตว์
คุณสมบัติเฉพาะ
• ชื่อสามัญ : Methane
• สูตรโมเลกุล : CH4
• น้ำหนักโมเลกุล : 16.04
• เป็นก๊าซเรือนกระจกที่ไม่มีสี ไม่มีกลิ่น ไม่มีรส
• จุดเดือด -161.5 °C
• จุดหลอมเหลว : 182.05 °C
• อุณหภูมิที่จุดไฟได้เอง : 640-840 °C
• อุณหภูมิเมื่อเผาไหม้ : 2,000 °C
• ค่าความร้อนจากการเผาไหม้ : 8,260 กิโลแคลอรี่/ลูกบาศก์เมตร
• ความสามารถการละลายน้ำ : 24×10-3 กรัม/ลิตร
• ละลายได้ดีในตัวทำละลายอินทรีย์ เช่น น้ำ มันเบนซิน อีเทอร์ และแอลกอฮอล์ เป็นต้น
ผลต่อภาวะเรือนกระจกของก๊าซต่างๆ
• CO2 = 1
• N2O = 230
• CH4 = 25
• CFCs = 15000
แหล่งกำเนิดก๊าซมีเทน
ก๊าซมีเทนที่พบในบรรยากาศส่วนใหญ่เกิดจากกระบวนการหมักอินทรียวัตถุแบบไม่ ใช้ออกซิเจน (anaerobic) ของจุลินทรีย์ พบการเกิดก๊าซได้มากบริเวณพื้นที่ที่มีน้ำขังหรือมีการหมักมมของสารอินทรีย์ เช่น นาข้าว แหล่งน้ำขัง ระบบบำบัดน้ำเสีย เป็นต้น แบ่งตามแหล่งเกิดได้ ดังนี้
กระบวนการเกิดก๊าซมีเทน
1. Fermentation หรือ Acedogenesis
จุลินทรีย์ย่อยสลายสารอินทรีย์โมเลกุลใหญ่ เช่น โปรตีน ไขมัน คาร์โบไฮเดรต ให้เล็กลงเป็นสารที่ละลายน้ำได้ กรดไขมัน กรดอะมิโน และน้ำตาล และถูกย่อยต่อจนเกิด Acetate และกรดไขมันที่ระเหยได้ที่มีคาร์บอนเป็นตัวเลขคี่มากกว่า Acetate เช่น โพรไพโอเนต (Propionate) และ บิวทิเรต (Butyrate) ซึ่งสารเหล่านี้ไม่สามารถถูกย่อยสลายได้โดย Methanogens และขณะย่อยสลายกรดไขมันจะทำให้เกิด ก๊าซไฮโดรเจน (H2)
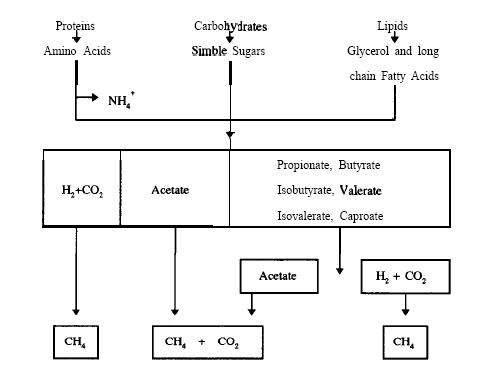
2. Syntrophic Acetigenesis
กรดไขมันที่ระเหยได้ที่มีคาร์บอนเป็นตัวเลขคี่มากกว่าสาม ซึ่งไม่ใช่ Acetate จะถูกย่อยสลายจนได้ Acetic acid และ CO2
3. Methanogenesis
เป็นกระบวนการเกิดก๊าซมีเทน แบ่งเป็น 2 กระบวนการที่สำคัญ คือ
– กระบวนการรีดักชั่นของคาร์บอนไดออกไซด์ (CO2 Reduction) โดยการใช้ก๊าซไฮโดรเจน (H2) ดังสมการ
CO2 + 4H2 → CH4 + 2H2O
– กระบวนการ Transmethylation ของกรดอะซิติก (Acetic acid) หรือเมทิลแอลกอฮอล์
(Methyl Alcohol) ดังสมการ
CH3COO– + H+ → CH4 + CO2
การแพร่ของก๊าซมีเทนออกสู่อากาศ
• รวมตัวกันเป็นฟองอากาศ แล้วปุดขึ้นเหนือน้ำออกสู่อากาศ
• โดยการแพร่ผ่านโมเลกุลน้ำขึ้นสู่ผิวน้ำ
• การแพร่ผ่านต้นพืช จากบริเวณราก ลำต้น และออกสู่อากาศบริเวณใบ และปากใบ
ประโยชน์ก๊าซมีเทน
ก๊าซมีเทน ถูกนำมาใช้อย่างมากสำหรับเป็นก๊าซหุงต้มเพื่อให้ความร้อนในการประกอบอาหาร และใช้เป็นก๊าซเชื้อเพลิงสำหรับเครื่องยนต์ต่างๆ
ก๊าซมีเทนที่เป็น ส่วนผสมในเชื้อเพลิงสำหรับเครื่องยนต์ เมื่อก๊าซมีเทน (CH4) ทำปฏิกิริยากับออกซิเจน (O2) ในห้องเผาไหม้อย่างสมบูรณ์จะเปลี่ยนเป็นก๊าซไฮโดรเจน (H2), ก๊าซคาร์บอนมอนนอกไซด์ (CO), ก๊าซคาร์บอนไดออกไซด์ (CO2), และน้ำ (H2O) ที่อุณหภูมิมากกว่า 1,000 K ดังสมการ
CH4 + O2 → CO2 + H2O
CH4 + H2O → CO + 3H2
CO + H2O → CO2 + H2
CH4 + 2H2O → CO2 + 4H2
ปฏิกิริยาก๊าซมีเทน
1. ปฏิกิริยาออกซิเดชั่นในบรรยากาศ
O + CH4 → H2 + H2CO
2. ปฏิกิริยากับสารอื่นๆในบรรยากาศ
OH + CH4 → CH3 + H2O
Cl + CH4 → HCl + CH3
CH4 +O2 → CH2O + H2O

