วัฏจักรไนโตรเจน (Nitrogen Cycle) หมายถึง การเปลี่ยนแปลงสภาพของธาตุไนโตรเจน และสารประกอบไนโตรเจนตามสภาพแวดล้อมที่แปรเปลี่ยนด้วยกระบวนการทางเคมี และการย่อยสลายของจุลินทรีย์ ทั้งในสิ่งมีชีวิต อากาศ ดิน หิน และน้ำ จากระบบหนึ่งไปสู่ระบบหนึ่ง หมุนเวียนเป็นวัฏจักร
ไนโตรเจนในอากาศ
ธาตุไนโตรเจนในอากาศ ถือเป็นแหล่งเริ่มต้นของวัฏจักรธาตุไนโตรเจน โดยพบมากที่สุดในอากาศถึงร้อยละ 78 จากปริมาตรอากาศทั้งหมด ในรูปของก๊าซไนโตรเจน (N2) นอกจากนั้น ยังพบในรูปของก๊าซอื่นๆ ได้แก่
– ก๊าซไนตริกออกไซด์ (Nitric oxide : NO
– ก๊าซไนตรัสออกไซด์หรือก๊าซหัวเราะ (Nitrous oxide : N2O)
– ก๊าซไนโตรเจนออกไซด์ (Nitrogen Oxide : NO2)
– ก๊าซ N2O4
– ก๊าซแอมโมเนีย (Ammonia : NH3)
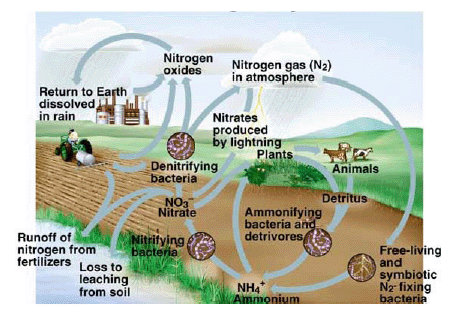
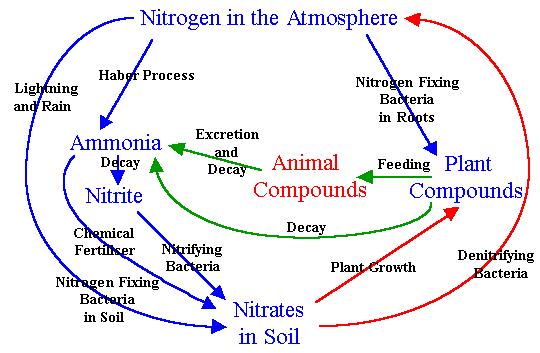
ก๊าซไนโตรเจนในรูปต่างๆ สามารถเกิดได้จากกระบวนการทางเคมี แบ่งได้ ดังนี้
1. กระบวนการย่อยสลายทางชีวภาพ
ไนโตรเจนที่พบเป็นองค์ประกอบของโปรตีนในพืช สัตว์ และจุลินทรีย์จะถูกย่อยสลายด้วยกระบวนการไฮโดรไลต์ โดยมีจุลินทรีย์บางชนิดเข้าร่วมซึ่งเป็นกระบวนการที่เกิดขึ้นในดิน และน้ำเป็นหลัก ตามสมการ
• โปรตีนในเนื้อเยื่อ → โปรตีโอส (proteoses) → เปปโตน (peptone) → เปปไตด์ (peptides)
• เปปไตด์ (peptides) → กรดอะมิโน (amino acid) → แอมโมเนีย (NH3) → แอมโมเนียม (NH4+)
• แอมโมเนียม (NH4+) + น้ำ (3H2O) → ไนเตรต (NO3–) → ไนไตรท์ (NO2–) → ไนตรัสออกไซด์ (N2O) → ก๊าซไนโตรเจน (N2)
จุลินทรีย์ที่เข้าย่อยสลายไนโตรเจนในรูปอินทรีย์สารให้เป็นอนินทรีย์สารจะเรียกกลุ่มจุลินทรีย์นี้ว่า แอมโมนิไฟเออร์ (ammonifiers) ซึ่งพบได้ในดินประมาณ 105-107 เซลล์/กรัมดินแห้ง
ในระหว่างการย่อยสลาย หากมีอออกซิเจนที่เพียงพอจะทำให้เกิดผลิตภัณฑ์ คือ คาร์บอนไดออกไซด์ (CO2) แอมโมเนีย (NH3) ซัลเฟต (SO4 2-) และน้ำ แต่หากมีออกซิเจนไม่เพียงพอจะเกิดคาร์บอนไดออกไซด์ (CO2) แอมโมเนีย (NH3) เอมีน (R-NH2) มีเทน (CH4) ไฮโดรเจนซัลไฟด์ (H2S) และกรดอินทรีย์ สังเกตได้จากดินมีกลิ่นเหม็นฉุน ส่วนในน้ำจะดำ และเหม็นเน่า
แอมโมเนีย (NH3) และก๊าซไนโตรเจน (N2) ถือเป็นผลิตภัณฑ์สุดท้ายของกระบวนการย่อยสลาย และการเปลี่ยนรูป โดยหลังจากกระบวนการย่อยสลายจนเกิดก๊าซแอมโมเนีย หากไม่สัมผัสกับน้ำก็จะระเหยออกสู่อากาศ แต่โดยมากจะเปลี่ยนรูปต่อเป็นไนเตรตจนได้ผลิตภัณฑ์สุดท้ายเป็นก๊าซไนโตรเจนในทีสุด
กระบวนการย่อยสลายสารอินทรีย์เป็นแอมโมเนีย แบ่งเป็น 2 กระบวนการ ดังนี้
1. แอมโมนิเซชัน (ammonization)
เป็นกระบวนการแรกของการย่อยสลายอินทรีย์วัตถุทั้งในดิน และน้ำ ด้วยจุลินทรีย์จนได้ผลิตภัณฑ์สุดท้ายเป็นเอมีน และกรดอะมิโน ดังสมการ
• โปรตีน → R-NH2 + CO2 + พลังงาน + ผลิตภัณฑ์อื่นๆ
2. แอมโมนิฟิเคชัน (ammonification)
เป็นกระบวนการต่อเนื่องจากแอมโมนิเซชัน ด้วยการย่อยสลายเอมีน และกรดอะมิโน จนได้ผลิตภัณฑ์สุดท้ายเป็นแอมโมเนีย แอลกอฮอล์ และพลังงาน ดังสมการ
• R-NH2 + H2O → R-OH + NH3 + พลังงาน
• 2NH3 + H2CO3 → (NH4)2CO3 + 2NH4+ CO32-
แอมโมเนียในขั้นตอนนี้มีทั้งระเหยสู่อากาศ ถูกพืชดูดไปใช้ และถูกตรึงในดินระหว่างอนุภาคดินเหนียว ซึ่งบางส่วนจะเข้าสู่การแปรสภาพเป็นไนเตรต และก๊าซไนโตรเจนต่อไป
กระบวนการทั้งสองจะเกิดขึ้นได้ดีในดิน และน้ำที่มีสภาพเป็นกลางได้ดีกว่าสภาพเป็นกรด เนื่องจากเป็นสภาวะที่จุลินทรีย์สามารถเติบโตได้ดีที่สุด รวมถึงในดินที่มีสภาพความชื้นที่เหมาะสม และสำหรับในดินที่มีน้ำขังหรือในน้ำที่ไม่มีออกซิเจนจะทำให้เกิดแอมโมเนียตกค้างจำนวนมาก เพราะขาดออกซิเจนสำหรับเข้าเปลี่ยนรูปแอมโมเนียเป็นไนเตรต นอกจากนี้ การเปลี่ยนแปลงอุณหภูมิอย่างรวดเร็วจะมีผลต่อการย่อยสลายด้วยเช่นกัน
การแปรสภาพแอมโมเนีย แบ่งเป็น 2 กระบวนการ ดังนี้
1. ไนตริฟิเคชัน (nitrification)
เป็นกระบวนการที่ต่อเนื่องจากแอมโมนิฟิเคชัน โดยใช้แอมโมเนียเป็นสารตั้งต้นสำหรับเปลี่ยนสภาพให้เป็นแอมโมเนียม ไนไตร์ท และไนเตรท ประกอบด้วย 2 ขั้นตอน ดังสมการ คือ
ขั้นแรก แอมโมเนีย/แอมโมเนียม ออกซไดซ์เป็นไนไตร์ท
• 2NH4+ + 3O2 → 2NO2- + 2H2O + 4H+ + พลังงาน
ขั้นที่ 2 ไนไตร์ทถูกออกซิไดซ์เป็นไนเตรท
• 2NO2- + O → 2NO3–
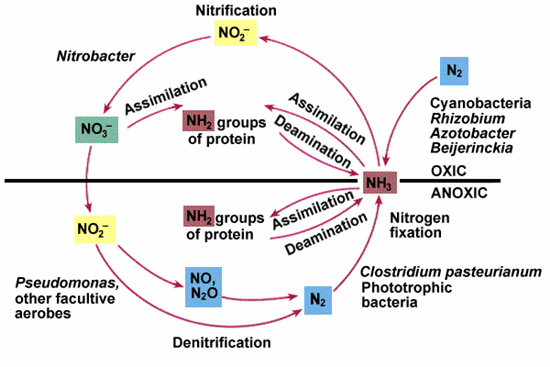
2. ดีไนตริฟิเคชัน (denitrification)
เป็นกระบวนการที่เกิดต่อเนื่องจากไนตริฟิเคชัน ด้วยการรีดิวซ์ไนเตรทให้เป็นไนไตร์ท ไนตรัสออกไซด์ และาซไนโตรเจนหรือไนตริกออกไซด์ปลดปล่อยสู่อากาศ ดังสมการ
• ไนเตรต (NO3–) → ไนไตรท์ (NO2–) → ไนตรัสออกไซด์ (N2O) → ก๊าซไนโตรเจน (N2)/ไนตริกออกไซด์ (NO)
โดยผลิตภัณฑ์ไนไตรท์ (NO2–) ที่เกิดในขั้นไนตริฟิเคชัน บางส่วนจะแปรรูปเป็นแอมโมเนียก่อนเข้าสู่กระบวนการรีดิวซ์อีกครั้ง และบางส่วนจะเข้าสู่กระบวนการรีดิวซ์เป็นก๊าซไนโตรเจนได้โดยตรง
2. กระบวนการเผาไหม้
การเผาไหม้ที่ไม่สมบูรณ์จากการเผาไหม้เชื้อเพลิง หรือซากพืช ซากสัตว์ ทำให้เกิดก๊าซของสารประกอบไนโตรเจน
• เชื้อเพลิง/วัตถุ + O2 → NO/NO2/N2O4
• แอมโมเนียมไนเตรต (
ไนโตรเจนในดิน
1. กระบวนการย่อยสลายทางชีวภาพ
การย่อยสลายของอินทรีย์วัตถุที่กล่าวข้างต้นในหัวข้อไนโตรเจนในอากาศจะเกิดสารประกอบอินทรีย์ไนโตรเจนรูปแบบต่างๆในดินที่สามารถย่อยสลายได้อย่างรวดเร็ว โดยขั้นสุดท้ายที่พืชสามารถนำไปใช้ประโยชน์ได้ คือ แอมโมเนีย (NH3) และ ไนเตรต (NO3-) ซึ่งสามารถอยู่ในดินได้จากแรงดึงดูดระหว่างอนุภาคดินเหนียว ก่อนบางส่วนจะเกิดปฏิกิริยาต่อกลายเป็นก๊าซไนโตรเจน
2. การตรึงไนโตรเจน
เป็นกระบวนการเปลี่ยนก๊าซไนโตรเจนในอากาศเป็นสารประกอบในโตรเจนที่พืชสามารถนำไปใช้ประโยชน์ได้ด้วยจุลินทรีย์ขนิด nitrogen fixing microorganism แบ่งการตรึงออกเป็น 2 แบบ คือ
• Symbiotic nitrogen fixation เป็นการตรึงไนโตรเจนจากอากาศแบบพึ่งอาศัยระหว่างจุลินทรีย์ และรากพืช โดยมีการสร้างบมบริเวณส่วนรากเพื่อเป็นที่อยู่ของแบคทีเรียสำหรับตรึง และเก็บกักเพื่อให้รากพืชดูดซึมไปใช้ประโยชน์ได้ จุลินทรีย์ที่พบ ได้แก่ ไรโซเบียม (Rhizobium) ส่วนพืชจะเป็นพืชตระกูลถั่ว เช่น ถั่วเขียว ถั่วเหลือง เป็นต้น
• Non-symbiotic nitrogen fixation เป็นการตรึงไนโตรเจนของจุลินทรีย์อิสระที่ไม่ต้องพึ่งแหล่งอาศัยเหมือนจุลินทรีย์แบบ Symbiotic nitrogen fixation
3. การใส่ปุ๋ย
รูปของธาตุไนโตรเจนที่สามารถอยู่ในดินได้จะเป็นสารประกอบของแข็งที่อยู่ในรูปปุ๋ยสำหรับใส่ให้แก่ต้นพืช ได้แก่
– ปุ๋ยแอมโมเนียมไนเตรต (ammonium nitrate, NH4NO3)
– ปุ๋ยโพแทสเซียมไนเตรท (potassium nitrate, KNO3)
– ปุ๋ยแคลเซียมไนเตรท (calcium nitrate, Ca(NO3)
สารประกอบของปุ๋ยเมื่ออยู่ในดิน และสัมผัสกับความชื้นจะแตกตัวให้ประจุไนเตรต (NO3–) ที่พืชสามารถดูดซึมไปใช้ได้
ไนโตรเจนในน้ำ
1. กระบวนการย่อยสลายทางชีวภาพ
การย่อยสลายของอินทรีย์วัตถุที่กล่าวข้างต้น สามารถเกิดในน้ำได้เช่นกัน จนได้สารประกอบไนโตรเจนรูปแบบต่างๆที่ละลายในน้ำ ทั้งในรูปของก๊าซ และของแข็งตกตะกอน ได้แก่
– ก๊าซแอมโมเนีย (NH3) ทีถูกตรึงอยู่ระหว่างอนุภาคของน้ำ แต่ส่วนมากจะออกสู่อากาศ
– ไนเตรต (NO3-) ที่เข้าจับกับเกลือที่ละลายในน้ำจนตกตะกอน เช่น แคลเซียม (Ca) ได้เป็นแคลเซียมไนเตรท (Ca(NO3), โพแทสเซียมไนเตรท (K) ได้เป็นโพแทสเซียมไนเตรท (KNO3) เป็นต้น
2. การละลายของออกไซด์ไนโตรเจน
– กรดไนตริก (HNO3) จากการละลายของไนโตรเจนไดออกไซด์ (NO2) ในน้ำ (2NO2 + H2O = HNO3 + HNO2)
สารประกอบของไนโตรเจนในน้ำบางส่วนจากกระบวนการย่อยสลาย และการละลายจากก๊าซจะเกิดปฏิกิริยาต่อกลายเป็นก๊าซไนโตรเจน (N2) เข้าสู่อากาศอีกครั้ง แต่บางส่วนจะรวมกับสารอื่นจนมีความเข้มข้นมากพอแล้วตกตะกอนในท้องน้ำ
ไนโตรเจนในพืช สัตว์ และจุลินทรีย์
ไนโตรเจนที่อยู่ในมนุษย์ สัตว์ พืช และจุลิทรีย์หรือสิ่งมีชีวิตขนาดเล็กจะได้รับจากสารอาหารที่กินหรือดูดซึมเข้าสู่ร่างกายหรือเซลล์ และเปลี่ยนให้อยู่ในรูปขององค์ประกอบของกรดอะมิโนที่เป็นโปรตีนในเซลล์ เมื่อสิ่งมีชีวิตตายไปก็จะเข้าสู่กระบวนการย่อยสลาย และกลับเข้าสู่วัฏจักรไนโตรเจนต่อไป
ดังนั้น วัฏจักรไนโตรเจน แบ่งได้เป็น 3 ส่วน คือ
1. ไนโตรเจนปฐมภูมิ/แหล่งไนโตรเจน เป็นแหล่งไนโตรเจนที่พบในอากาศ
2. ไนโตรเจนทุติยภูมิ/ไนโตรเจนย่อยสลาย เป็นแหล่งไนโตรเจนที่พบในดิน หิน และน้ำ
3. ไนโตรเจนตติยภูมิ/ไนโตรเจนเก็บกัก และใช้ประโยชน์ เป็นแหล่งไนโตรเจนที่พบในสิ่งมีชีวิต เช่น มนุษย์ สัตว์ พืช และจุลินทรีย์

